Spis treści:
Unikalna Identyfikacja Wyrobów Medycznych (UDI) to system służący oznaczaniu i identyfikacji urządzeń medycznych w łańcuchu dostaw opieki zdrowotnej w wymiarze globalnym.
Co to jest Unikalna Identyfikacja Wyrobów Medycznych – UDI?
Przed wprowadzeniem do obrotu wyrobów, do których ma zastosowanie system UDI, producent jest zobowiązany do nadania wyrobowi oraz – w stosownych przypadkach – wszystkim wyższym poziomom opakowania, niepowtarzalnego kodu identyfikacyjnego wyrobu (UDI). UDI musi być kodem utworzonym zgodnie z zasadami podmiotu wydającego wyznaczonego przez Komisję do prowadzenia systemu nadawania kodów UDI. GS1 jest agencją akredytowaną przez FDA (wrzesień 2013) oraz przez KE (czerwiec 2019) dla celów UDI.
Na czym polega UDI?
System UDI ułatwi identyfikowalność wyrobów medycznych, znacznie zwiększy skuteczność działań związanych z bezpieczeństwem po wprowadzeniu wyrobów do obrotu i pozwoli na lepsze monitorowanie przez właściwe organy. Pomoże również zmniejszyć błędy medyczne i walczyć z procederem fałszowania wyrobów. Zastosowanie systemu UDI powinno usprawnić zakupy i zasady utylizacji oraz zarządzanie zapasami przez instytucje opieki zdrowotnej i inne podmioty gospodarcze.
System UDI obejmuje:
- utworzenie kodu UDI zawierającego identyfikator urządzenia UDI (UDI-DI) specyficzny dla producenta i wyrobu, identyfikator produkcji UDI (UDI-PI), który identyfikuje jednostkę produkcji wyrobu
- umieszczenie nośnika UDI na etykiecie wyrobu lub na opakowaniu lub w przypadku wyrobów wielokrotnego użytku na samym urządzeniu (znakowanie bezpośrednie)
- przechowywanie kodu UDI przez podmioty gospodarcze, instytucje zdrowia publicznego i pracowników służby zdrowia,
- utworzenie elektronicznej bazy danych Unikalnej Identyfikacji Wyrobów Medycznych (baza danych UDI), która jest częścią bazy danych EUDAMED (Europejska Baza Danych Urządzeń Medycznych).
W UE producent przypisuje swoim wyrobom razem z UDI również Basic UDI-DI, który nie jest jeszcze wymagany przez inne jurysdykcje. Kod Basic UDI-DI jest głównym identyfikatorem modelu wyrobu – jest kluczowym elementem umożliwiającym łączenie różnych modułów Europejskiej Bazy Danych o Wyrobach Medycznych (EUDAMED). Jest to główny klucz umożliwiający wprowadzenie informacji do bazy danych UDI i jest on wskazywany w odpowiednich certyfikatach i deklaracjach zgodności UE. Służy do rejestracji wyrobów medycznych i jest przydzielany niezależnie od opakowania/etykiety, nie pojawia się na żadnej jednostce handlowej, a także różni się od identyfikatora jednostek handlowych w łańcuchu dostaw (UDI-DI / GTIN). Każdy kod Basic UDI identyfikuje wyrób w unikalny sposób.
Z czego jest zbudowany kod zgodny z wytycznymi Unikalnej Identyfikacji Wyrobów Medycznych?
UDI to ciąg znaków numerycznych lub alfanumerycznych, który jest stworzony za pomocą globalnie akceptowanego urządzenia służącego do identyfikacji i zgodnie ze standardem kodowania. Pozwala na jednoznaczną identyfikację określonego wyrobu medycznego na rynku. Kod UDI jest nadawany samemu wyrobowi lub jego opakowaniu. Wyższe poziomy opakowania (karton, skrzynka) mają własne kody UDI. Jednostki logistyczne nie podlegają wymogom dotyczącym kodu UDI. Jak wspomniano wcześniej, składa się z dwóch części: kodu UDI-DI oraz kodu UDI-PI.
Kod UDI-DI
Kod UDI-DI jest niepowtarzalnym kodem numerycznym lub alfanumerycznym właściwym dla danego modelu wyrobu, używanym również jako „klucz dostępu” do informacji przechowywanych w bazie danych UDI. UDI-DI jest niepowtarzalny na każdym poziomie opakowania wyrobu.
Kod UDI-PI
Kod UDI-PI jest niepowtarzalnym kodem numerycznym lub alfanumerycznym identyfikującym jednostkę produkcji wyrobu. Różne rodzaje kodu UDI-PI obejmują numer seryjny, numer serii, identyfikację oprogramowania oraz datę produkcji lub datę ważności, lub obie te daty.
Jeżeli na etykiecie znajduje się numer serii, numer seryjny, identyfikacja oprogramowania lub data ważności, stanowią one część kodu UDI-PI. Jeżeli na etykiecie znajduje się także data produkcji, nie musi ona być włączona do kodu UDI-PI. Jeżeli zaś na etykiecie znajduje się jedynie data produkcji, jest ona używana jako kod UDI-PI.
Każdej części składowej, która jest uznawana za wyrób i jest oddzielnie dostępna w handlu, nadaje się oddzielny kod UDI, chyba że te części składowe są częścią wyrobu konfigurowalnego, który jest oznaczony własnym kodem UDI.
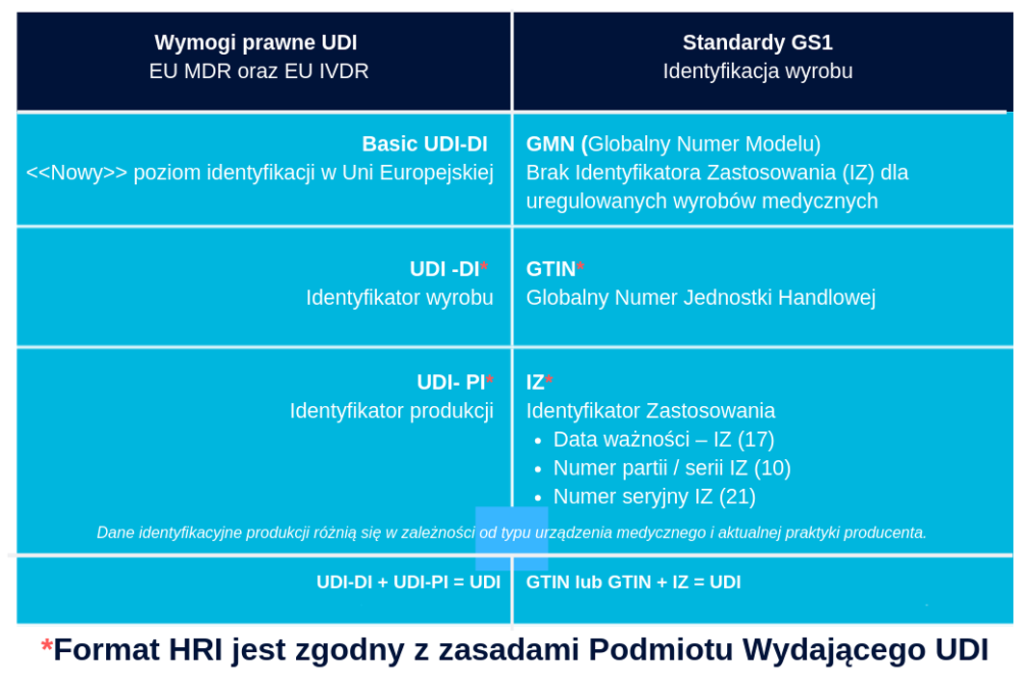
Wg standardu kodowania GS1, UDI-DI (Identyfikator wyrobu) to GTIN, czyli Globalny Numer Jednostki Handlowej; UDI-PI (Identyfikator produkcji) to IZ – Identyfikator Zastosowania:
- Data ważności IZ(17)
- Numer partii/serii IZ(10)
- Numer seryjny IZ(21)
Basic UD-DI odpowiada GMN (Globalny Numer Modelu). (Rys. 1 )
Zastosowanie UDI dla urządzeń medycznych
System UDI ma zastosowanie do wszystkich urządzeń z wyjątkiem wykonanych na zamówienie oraz urządzeń badawczych. Producent jest odpowiedzialny za przestrzeganie wszystkich wymagań związanych z UDI. Obejmuje to przypisanie UDI (i Basic UDI-DI), rejestrację UDI (i Basic UDI-DI) w bazie danych EUDAMED i umieszczenie nośnika UDI na etykiecie wyrobu lub na jego opakowaniu lub, w przypadku wyrobów wielokrotnego użytku, na samym urządzeniu (znakowanie bezpośrednie).
W jaki sposób UDI powinien pojawić się na etykiecie?
Nośnik UDI (Automatyczna Identyfikacja i zbieranie danych AIDC i interpretacja czytelna dla człowieka HRI) powinien znajdować się na etykiecie lub na samym wyrobie i na wszystkich wyższych poziomach opakowania urządzenia. Nośniki UDI zawierają m.in. kod kreskowy 1D/liniowy, kod kreskowy 2D/matrycowy, RFID. Rys. 2
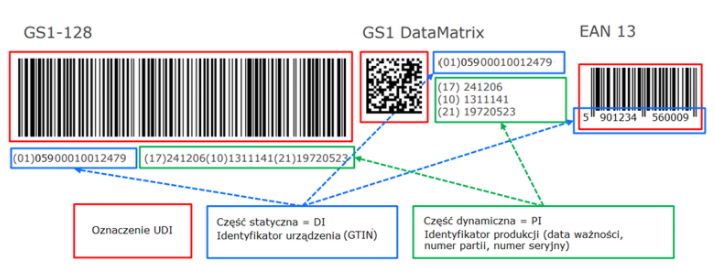
Nośnikiem kodu UDI może być, zgodnie z wytycznymi GS1, np. kod GS1-128, który zawiera część statyczną w postaci GTIN (ID – identyfikator wyrobu), przy czym GTIN składa się z cyfr oznaczających kolejno: krajowy prefiks (dla Polski 59), prefiks firmy, oznaczenie produktu oraz cyfra kontrolna oraz część dynamiczną ((PI – identyfikator produkcji) jak data ważności, numer serii, numer seryjny.
Kolejnym przykładem nośnika kodu UDI jest kod dwuwymiarowy – GS1 DataMatrix zawierający GTIN – identyfikator wyrobu (ID) oraz identyfikator produkcji (IP); sam EAN-13 zwierający GTIN będący identyfikatorem wyrobu (ID).
W przypadku braku miejsca na opakowaniu jednostkowym wyrobu, nośnik UDI można umieścić na kolejnym wyższym poziomie pakowania. Wyższe poziomy opakowań mają swój własny niepowtarzalny kod UDI. Należy pamiętać, że opakowania transportowe są zwolnione z wymagań.
Kod UDI musi mieć postać zwykłego tekstu/ czytelną dla człowieka informację (HRI) oraz w formie wykorzystującej technologię AIDC. Jeśli istnieją znaczne ograniczenia miejsca na etykiecie dla pojawienia się obu wersji kodu – HRI i AIDC- wtedy wymagany jest tylko format AIDC. W przypadku wyrobów przeznaczonych do użytku poza placówkami służby zdrowia, np. jako urządzenia do opieki domowej, HRI musi jednak pojawić się na etykiecie, nawet jeśli powoduje to brak miejsca na format AIDC.
AIDC jest technologią używaną do automatycznego zbierania danych. Technologie AIDC obejmują kody kreskowe, karty chipowe, biometrię i RFID.
Producenci mogą używać jedynie standardów kodowania przygotowanych przez podmioty wydające wyznaczone przez Komisję (w tym przypadku GS1).
Standardy GS1 a UDI
Standardy Systemu GS1 mają zasadnicze znaczenie z punktu widzenia umożliwienia skutecznego i efektywnego wdrażania UDI przez wszystkich interesariuszy na całym świecie. System standardów GS1 wspiera wszystkie zainteresowane strony w wydajnym i skutecznym spełnianiu wymagań UDI, umożliwiając interoperacyjność i zgodność w ramach organizacji, między organizacjami i ponad granicami. Jeden wspólny standard może ostatecznie przyspieszyć wdrożenie i zwiększyć zgodność z przepisami UDI. GS1 ma 114 organizacji członkowskich GS1 i ponad 2700 pracowników na całym świecie, którzy zapewniają użytkownikom wsparcie w zakresie wdrażania UDI w ich ojczystym języku i zrozumienia lokalnych wymagań dotyczących wdrożenia. (źródło: www.gs1pl.org)
W rozporządzeniu (UE) nr 2017/745[17] i rozporządzeniu (UE) nr 2017/746[18] ustanowiono przepisy dotyczące wprowadzania do obrotu wyrobów medycznych i do diagnostyki in vitro oraz badań klinicznych. Wyroby pogrupowano, uwzględniając przewidziane zastosowanie wyrobów orazzwiązane z nimi ryzyko, wyróżniając 4 klasy: I, IIa, IIb oraz III. Klasyfikacja wyrobu odbywa się wg 22 reguł klasyfikacyjnych.
W związku z Rozporządzeniem Parlamentu Europejskiego i Rady (UE) 2017/745 z dnia 5 kwietnia 2017 r. UDI musi zacząć być obowiązkowo umieszczany na etykiecie wyrobu w zależności od jego klasy w następujących terminach:
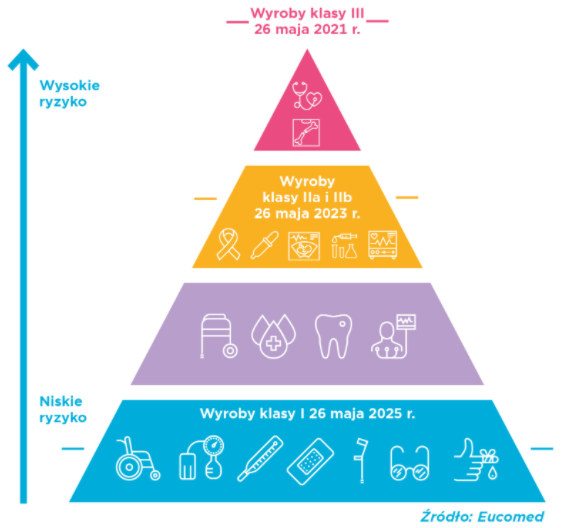
Produkty klasy I z najniższym ryzykiem to np. kołnierze ortopedyczne, rękawice do badań, wózki inwalidzkie, bandaże elastyczne, nici dentystyczne, wyroby z funkcją pomiarową, wyroby sterylne, skalpel, gips;
Produkty klasy IIa to np. opatrunki hydrożelowe, cewniki jednorazowe, klisze rentgenowskie, implanty zębów, strzykawki; klasa IIb to np. pojemniki na krew, prezerwatywy czy respiratory. Klasa III, produkty o największym ryzyku, to np. implanty piersi, zastawki serca, protezy naczyniowe, implanty ślimakowe, baterie do rozruszników serca.
Znakowanie kodu UDI w praktyce
Zgodnie z zasadą, iż użytkownik końcowy powinien mieć możliwość identyfikacji wyrobu przy pomocy kodu UDI, należałoby rozpocząć znakowanie już od opakowania indywidualnego poszczególnych wyrobów (w przypadku wyrobów jednorazowego użytku pakowanych w opakowania jednostkowe). Bo nawet jeśli w przypadku wyrobów jednorazowego użytku klas I i IIa pakowanych i oznakowanych pojedynczo nie wymaga się, aby nośnik kodu UDI występował na opakowaniu, a jedynie znalazł się na wyższym poziomie opakowania, np. kartonie zawierającym kilka wyrobów pakowanych indywidualnie, to w sytuacji, gdy produkt ten będzie stosowany w warunkach domowych i nie będzie dostępu do wyższego poziomu opakowania wyrobu (kartonu), kod UDI umieszcza się na opakowaniu indywidualnym poszczególnych wyrobów.
W przypadku wyrobów przeznaczonych wyłącznie do punktów sprzedaży detalicznej, nie wymaga się wprawdzie umieszczania kodów UDI-PI w formacie AIDC na opakowaniu do sprzedaży detalicznej, jednak wymagane jest oznakowanie w formacie HRI (czytelne dla człowieka).
Zintegrowane rozwiązania zapewniające zgodność z UDI
Markem-Imaje wspomaga producentów wyrobów medycznych w przestrzeganiu przepisów, które wymagają zastosowania unikalnego identyfikatora dla każdego produktu schodzącego z linii produkcyjnej. Markem-Imaje tworzy w tym zakresie partnerstwo z liderami branży takimi jak Bosch, Cognex i HP, dostarczając walidowane rozwiązania pod klucz do druku i kontroli wizyjnej. Całość obsługiwana jest przy pomocy jednego interfejsu operatora i zarządzana przez oprogramowanie sieciowe CoLOS.
Przykłady zintegrowanych rozwiązań dla celów UDI wykorzystujących urządzenia, oprogramowanie Markem-Imaje oraz partnerstwo z producentami maszyn pakujących:
Rozwiązanie do drukowania i walidowania komunikatów
Markem-Imaje opracował, we współpracy z Bosch Packaging Technology, zintegrowane rozwiązanie do drukowania i walidowania komunikatów zgodnych z UDI, na torbach Tyvek, foliach, torbach foliowych, kartonikach, blistrach i etykietach. Komunikaty po nadruku weryfikowane są przez zintegrowany system wizyjny CoLOS Mark&Read, a w przypadku błędu odrzucane. Wszystkie dane przechowywane są w terminalu CoLOS. W rozwiązaniu pod klucz wykorzystana została termiczna drukarka atramentowa wysokiej rozdzielczości serii Markem-Imaje 1050, oprogramowanie CoLOS Mark&Read oraz zgrzewarka Bosch.
“Markem-Imaje jest dla nas niezawodnym dostawcą i w wielu przypadkach zaprojektowało sprzęt specjalnie przeznaczony do montażu w naszych urządzeniach. Okazali się bardzo pomocni i są bardzo dobrym partnerem” powiedział Ray Johnson, Manager Produktu, Bosch.

System pakowania i znakowania
Kolejny przykład rozwiązania pod klucz dla producentów wyrobów medycznych to system pakowania i znakowania, składający się z maszyny zgrzewającej poziomej Alpha VII firmy Formost Fuji (USA), oprogramowania CoLOS Marke&Read oraz drukarki termotransferowej SmartDate X60 Markem-Imaje. Rozwiązanie CoLOS Mark&Read wykorzystuje dotykową konsolę z komputerem PC i obsługuje zintegrowany system wizyjny Cognex, który pozwala czytać i weryfikować kody 2D oraz opis czytelny dla człowieka, i który może przechowywać wszystkie informacje w terminalu CoLOS. Drukarka i system wizyjny programowane są równocześnie po wybraniu zadania do druku, dzięki czemu użytkownik nie musi obsługiwać wielu urządzeń i interfejsów jednocześnie. Takie rozwiązanie znacznie ułatwia producentom konfigurowanie, weryfikację i obsługę. Otrzymują właściwy komunikat, na właściwym produkcie i we właściwym czasie.
Sposoby nanoszenia kodu UDI
Mówiąc o znakowaniu opakowań kodem UDI, należy wspomnieć o dwóch sposobach nanoszenia kodu – druk na etykiecie oraz znakowanie bezpośrednio na opakowaniu. (Rys. 4)
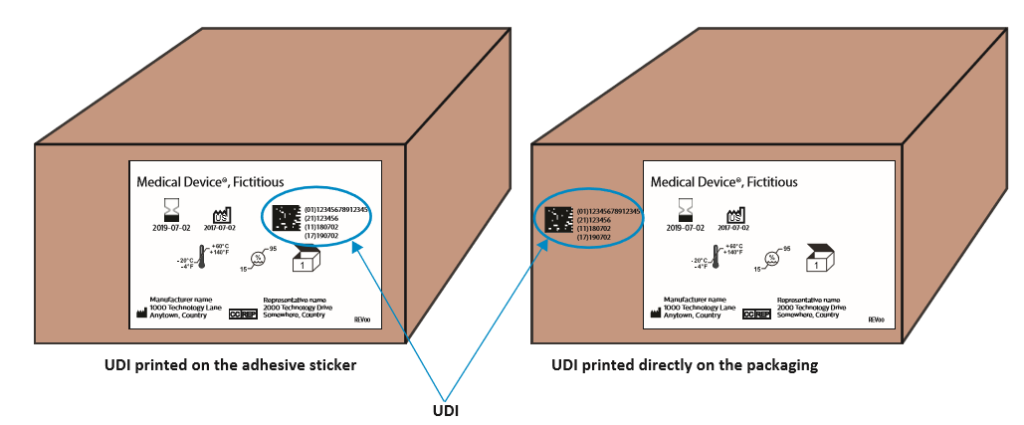
- W przypadku opcji pierwszej stosowne będzie użycie systemu drukująco-etykietującego Markem-Imaje 2200. To elastyczne, kompaktowe rozwiązanie do automatycznego druku i etykietowania opakowań zbiorczych spełnia wymogi jakościowe GS1 stawiane kodom kreskowym, stąd pewność, że kod GS1-128 czy GS1- DataMatrix będą wygenerowane i wydrukowane poprawnie. Klasa kodu jest w przypadku technologii druku termotransferowego wysoka i ma wartość A.
- Podobnie skutecznym i estetycznym, a przy tym ekonomicznym sposobem nadruku jest druk bezpośrednio na kartonie. Markem-Imaje posiada opatentowaną technologię druku tuszem termoelastycznym TouchDry® zaimplementowaną w drukarkach woskowych wysokiej rozdzielczości 5800– nadruki i kody nie blakną, nie migrują w głąb podłoża, pozostają wyraźne, trwałe, kontrastowe przez wiele lat, w przeciwieństwie do kodów naniesionych przy użyciu drukarek atramentowych wysokiej rozdzielczości, gdzie absorbcja atramentu przez karton wpływa na pogorszenie jakości kodu kreskowego. Z uwagi na ciemne podłoże kartonu, przeciętna klasa kodu, jaką możemy uzyskać przy nadrukach bezpośrednio na kartonie z wykorzystaniem drukarki woskowej 5800 to C. Tu, podobnie jak w systemie Markem-Imaje 2200, mamy pewność zgodności kodów z wymogami GS1, gdyż obydwa urządzenia wykorzystują to samo oprogramowanie CoLOS.
W przypadku wyrobów medycznych wielokrotnego użytku, system UDI nakłada na producentów obowiązek trwałego znakowania wyrobu. W przypadku wyrobów wielokrotnego użytku, które wymagają czyszczenia, dezynfekcji, sterylizacji lub odtworzenia między zastosowaniami u pacjentów, nośnik kodu UDI ma być trwały i czytelny po każdym wykonanym zabiegu służącym przygotowaniu wyrobu do następnego użycia przez przewidziany okres używania wyrobu.
Laser XENO firmy CAB, jako kompaktowe, bezpieczne urządzenie, wraz z oprogramowaniem cabLase pozwoli na trwałe znakowanie wyrobów medycznych wielokrotnego użytku jak np. narzędzia chirurgiczne. XENO 1 spełnia wysokie standardy przemysłowe, jest laserem klasy 1 i jednocześnie jest przyjazny i wygodny w obsłudze.

Tekst opracowano na podstawie ogólnodostępnych materiałów; nie stanowi on porady prawnej.
—————————————————————————————————————————————–
Źródła:
Rozporządzenie Parlamentu Europejskiego i Rady Unii Europejskiej z 5 kwietnia 2017 roku. (745/2017);
www.gs1pl.org
www.markem-imaje.com
Unique Device Identification system (UDI system) Application Guide opublikowany przez International Medical Device Regulators Forum 2019 r.
http://www.imdrf.org/docs/imdrf/final/technical/imdrf-tech-190321-udi-sag.pdf
https://ec.europa.eu/docsroom/documents/42641